Температура замерзания воды

Свойства воды
Как вы думаете, вода всегда замерзает при 0°С? Ну, это не совсем так. На самом деле чистая вода может замерзнуть даже при более низких температурах, вплоть до -42°C. Однако для формирования кристаллов льда ему нужна основа, которой может быть что угодно — от частиц пыли до пузырьков воздуха или трещин в контейнере с водой.
Это означает, что чистая вода без каких-либо посторонних частиц может вообще не замерзнуть при 0°С. Кроме того, степень солености воды может напрямую влиять на ее температуру замерзания: чем больше соли, тем ниже температура, необходимая для замерзания.
Температура замерзания пресной воды — 0 °C.
Например, океанская вода начинает замерзать при температуре около -1,9°C. Но как насчет рыбы? Те, что обитают в полярных морях, имеют температуру замерзания крови -0,5°C, достигаемую за счет белков в их крови, которые подавляют процесс кристаллизации.
Вода на планете
Значение воды на нашей планете неизмеримо, так как это не только одно из самых существенных, но и самых замечательных явлений. Вода играет важнейшую роль в возникновении и продолжении жизни на Земле, в химическом составе живых организмов, в формировании погоды и климата. Таким образом, вода является самым важным веществом для всех живых существ на планете.
Большая часть поверхности Земли покрыта водой, включая океаны, моря, озера, реки и лед. Примерно 96,5 % воды Земли находится в океанах, 1,7 % — в подземных запасах, еще 1,7 % — в ледяных шапках и ледниках Антарктиды и Гренландии, небольшая часть — в реках, озерах и болотах. Только 0,001% воды находится в облаках, которые образуются из льда и жидких частиц воды, взвешенных в атмосфере.
При нормальных условиях вода находится в жидком состоянии, но при температуре 0°С застывает в лед, а при 100°С закипает и превращается в водяной пар.
При создании температурной шкалы Цельсия температуры таяния льда и кипящей воды использовались для определения значений 0°C и 100°C соответственно.
Лед можно найти в различных формах в природе, таких как материк, плавающий, подземный, снежный, иней и иней. Под действием собственного веса лед становится пластичным и текучим.
Природный лед, как правило, намного чище воды, потому что первые молекулы, которые входят в решетку при кристаллизации воды, — это молекулы воды.
На Земле имеется около 30 миллионов км³ общих запасов льда, большая часть из которых расположена в полярных шапках, особенно в Антарктиде, где толщина ледяного слоя может достигать 4 км.
В океанах соленая вода препятствует образованию льда, поэтому лед образуется только в полярных и субполярных регионах с продолжительными и очень холодными зимами. Некоторые мелководные моря в умеренном поясе также замерзают.
Кроме того, лед был обнаружен на планетах Солнечной системы, таких как Марс, его спутники, карликовые планеты и ядра комет.
Понимание свойств воды имеет решающее значение для прогресса человечества.
Свойства замерзшей воды
Кроме того, вода способна разрушать под своим воздействием особенно твердые породы. Одним из уникальных свойств воды при замерзании является ее расширение, позволяющее льду плавать на воде в жидком состоянии.
Как физическое вещество вода имеет сильное сродство к самой себе, большее, чем любая другая жидкость. Это свойство заставляет воду образовывать сферические капли на поверхностях, поскольку сферы имеют наименьшую площадь поверхности для данного объема.
Самая высокая плотность воды возникает при 4 градусах Цельсия, а замерзает она при нуле градусов Цельсия.
Однако морская вода замерзает при более низкой температуре -1,9 градуса по Цельсию из-за ее солености.
Вода обладает высокой теплоемкостью, то есть она относительно мало нагревается при повышении температуры. Кроме того, вода обладает высокой скрытой теплотой плавления (около 80 кал/г) и испарения (около 540 кал/г), позволяя ему поглощать значительное количество тепловой энергии.
Вода также имеет постоянную температуру при кипячении или замерзании.
Дистиллированная вода имеет низкую способность проводить электричество, но наличие даже небольшого количества солей может значительно увеличить ее проводимость.
При смешивании соли со снегом происходят два процесса — кристаллическая структура соли разрушается с поглощением тепла, а ионы гидратируются, выделяя тепло в окружающую среду. Для поваренной соли и хлористого кальция преобладает разрушение кристаллической структуры, приводящее к активному отводу тепла из окружающей среды.
Солевые растворы имеют температуру замерзания ниже 0 градусов по Цельсию, поэтому их используют для таяния снега на тротуарах при отрицательных температурах.
Снег обладает уникальным свойством под названием «память» и может сохранять информацию. Например, глубина и давление следов животных, оставленных на снегу, могут научить нас физике.
Более крупные животные оставляют более глубокие следы, а более мелкие оставляют неглубокие.
Опыт — замерзание соленой воды
Чтобы заморозить соленую воду, наполните две формы чистой водой и очень соленой водой. Поместите формы в холод или морозильную камеру. Вы заметите, что чистая вода замерзает, а соленая вода замерзает только при очень низких температурах. Хотя вода обычно имеет наибольшую плотность при 4 градусах Цельсия, она замерзает при нуле градусов Цельсия.
 Пресная и соленая вода — начало опыта
Пресная и соленая вода — начало опыта  Пресная и соленая вода — после замерзания. Пресная вода замерзла быстрее.
Пресная и соленая вода — после замерзания. Пресная вода замерзла быстрее.
Однако морской лед ведет себя иначе, чем пресноводный лед. По мере увеличения солености температура замерзания соленой воды снижается. Температура замерзания колеблется от -1,6 до -1,9 градусов по Цельсию при уровне солености от 30 до 35 частей на миллион.
Образование морского льда можно рассматривать как замерзание пресной воды, но соли вытесняются в ячейки морской воды внутри ледяной массы. Когда температура достигает точки замерзания, образуются кристаллы льда, которые покрывают незамерзшую воду.
Замерзание дистиллированной воды
При температуре -42 °С дистиллированная вода замерзает из-за отсутствия в ней примесей и других компонентов, которые могли бы послужить зародышами для кристаллизации. После прохождения нескольких ступеней очистки дистиллированная вода освобождается от таких веществ. На самом деле современным ученым удалось очистить воду до такой степени, что она замерзает только при -70°С. Это невероятное свойство принесло ей название переохлажденной воды.
Интересно, что если в дистиллированную воду добавить даже небольшое количество снега, песка или льда, то под действием низкой температуры она моментально замерзнет в красивые длинные кристаллы.
Замерзание соленой воды
Когда очищенная вода замерзает при очень низких температурах, соленая вода замерзнет при температуре -1,9 градуса по Цельсию. Однако индекс замерзания воды непостоянен из-за различных факторов, таких как концентрация солей и территориальное расположение.
Каспий замерзает при -0,5 градуса по Цельсию, Азовское море при -0,7 градуса по Цельсию, а Японское море не замерзает вообще из-за чрезвычайно высокого содержания соли в нем — 34 промилле. Балтийское море и пресные водоемы замерзают при 0 градусов по Цельсию.

Каспийское море начало замерзать
Ученые установили, что средняя скорость замерзания воды во всех морях составляет -4 градуса по Цельсию.
Интересные факты включают в себя способность соли заставлять воду замерзать при температуре -21 градус Цельсия, а также плавить лед. Холодная вода замерзает медленнее, чем горячая при низких температурах. Только 3% мировой воды пригодно для питья, а вода с добавлением метана будет гореть. Электрическое поле может удерживать воду в жидком состоянии при низких температурах. Лед содержит пузырьки воздуха и не тонет, поэтому вода под ним не замерзает.
Заключение
В заключение следует отметить, что температура замерзания воды зависит от концентрации примесей и солей в ее химическом составе и других факторов, таких как территориальное расположение.
Какая вода замерзает быстрее: горячая или холодная?
Не такой уж простой вопрос, как может показаться на первый взгляд. Споры о том, какая вода замерзнет быстрее, ведутся еще со времен Аристотеля! Давайте разбираться.


Поворотным моментом в истории изучения замерзания воды стал эксперимент с мороженым.
С чего все началось?
В 1963 году старшеклассник Эрасто Мпемба из Танзании случайно обнаружил эффект, позднее названный в его честь. Рассказываем, как он к этому пришел. Школьники учились готовить мороженое (нам бы такие уроки!). Эрасто переживал, что ему не хватит места в морозильнике, поэтому поставил свою заготовку еще горячей. Одноклассники же наоборот дали смесям остыть и только после этого отправили их в морозилку. В итоге мороженое из теплого молока получилось быстрее, чем из охлажденного. Эрасто поспешил за объяснением к учителю физики, но тот только посмеялся над ним, сказав: “ Это не всемирная физика, а физика Мпембы ”.

© Saskatchewan Science Centre/youtube.com
Кто провел первые лабораторные эксперименты?
Мпемба не бросил попыток выяснить, в чем дело, и позднее обратился за помощью к физику Денису Осборну. Вместе они провели первые систематические научные исследования феномена – эффекта Мпембы. Им удалось воспроизвести результат, хотя опытный Осборн отметил, что для полного понимания происходящего нужно провести более сложные эксперименты. За прошедшие десятилетия многие ученые и лаборатории пытались раскрыть загадку эффекта Мпембы, но получали неоднозначные результаты.
Казалось бы, эффект легко проверить. Берем чашки с горячей и холодной водой, ставим их в морозилку и засекаем время. Аристотель, Рене Декарт и Фрэнсис Бэйкон замечали, что горячая вода замерзает быстрее. Даже современные водопроводчики утверждают, что зимой трубы с горячей водой лопаются чаще, чем трубы с холодной.
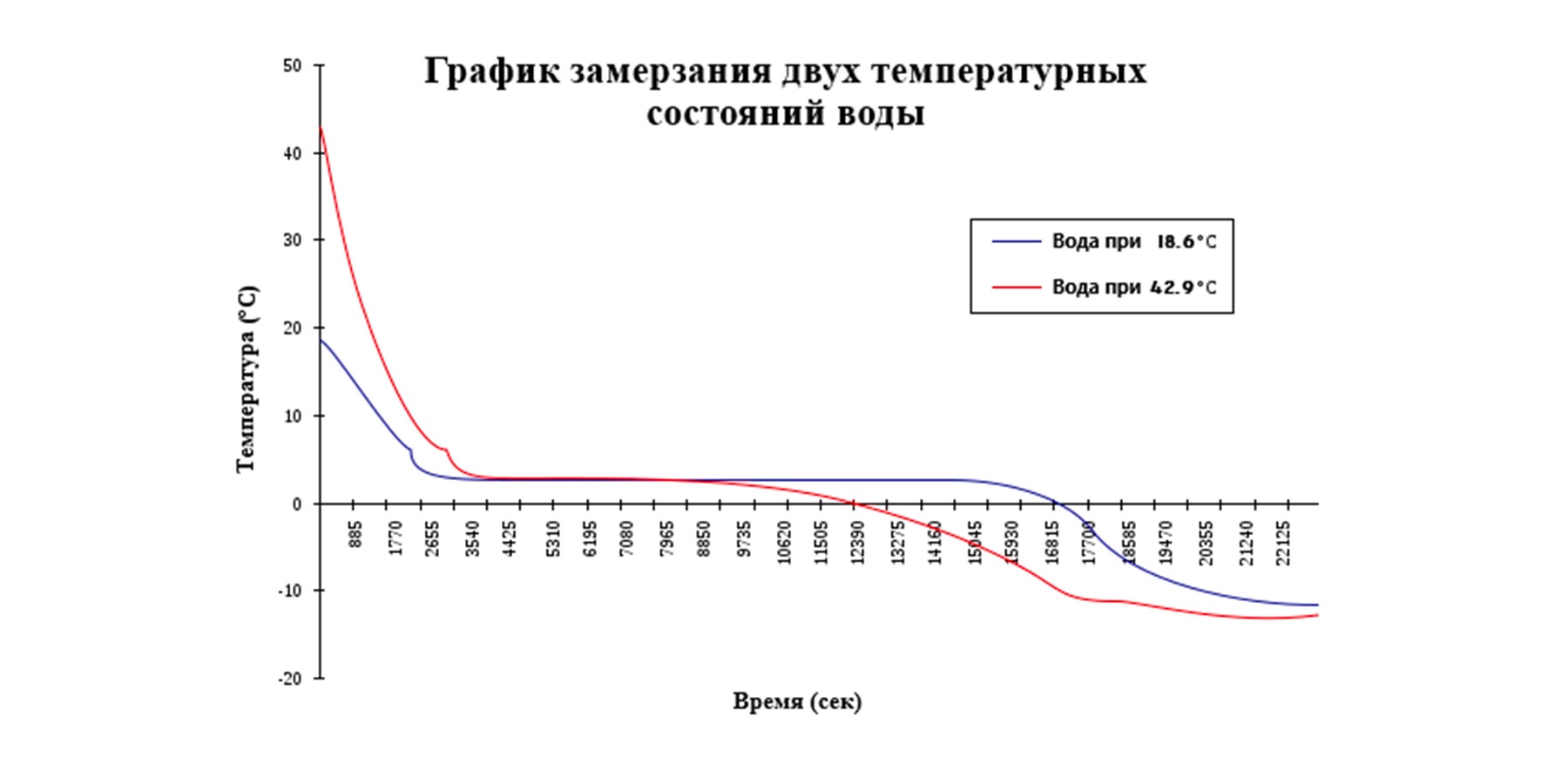
Результаты эксперимента с замораживанием двух образцов в разное время. Обнаружена разница в скорости замерзания.
Удалось ли другим ученым повторить эксперименты и получить “эффект Мпембы”?
Шло время, появлялись новые гипотезы, и ученые проверяли их в максимально контролируемых условиях. Некоторые из них обнаружили эффект, другие – нет. Почему? Дело в том, что замерзание воды – достаточно непредсказуемый процесс. Особенно когда речь идет о долях секунд и температур.
Начнем с базовой физики. Неважно, какая у воды стартовая температура. Чтобы превратиться в лед, вода сперва должна охладиться до нуля градусов. В процессе замерзания температура воды будет оставаться неизменной. Почему же тогда горячая вода в некоторых экспериментах замерзала быстрее холодной?

Эффект Мпебы зимой (эксперимент с замерзанием горячей воды на морозе)
Как пробовали объяснить “эффект Мпембы”?
Существует несколько гипотез.
Горячая вода быстрее испаряется, а значит в процессе охлаждения ее объем может сократиться – поэтому она быстрее замерзнет.
С другой стороны лед в морозильнике может играть роль изолятора. Холодной чашке он будет мешать быстро охладиться, а вокруг горячей растает: чашка коснется охлаждающих элементов морозильника и быстрее остынет.
Также роль могут сыграть газы. В холодной воде больше растворенных газов, чем в горячей, и это может сыграть роль при охлаждении.
А вот твердые примеси могут повлиять на само замерзание. Помните популярные видео с бутылкой жидкой воды, которая при ударе начинает затвердевать на глазах? Эту воду аккуратно охладили ниже температуры замерзания, и в ней не образовались центры кристаллизации. Возможно, в спокойных условиях холодной воде требуется сильнее сверхохладиться, чтобы запустилась кристаллизация?
Наконец, существует гипотеза о влиянии конвекции. Теоретически, горячая вода может быстрее охлаждаться, потому что в ней сильнее потоки теплообмена.
Это разумные предположения, но их можно исключить: использовать герметичные контейнеры, очистить морозильник ото льда, проверить содержание примесей и так далее. И даже с учетом этих факторов эффект Мпемба то подтверждается, то нет. Как же так? Дело в том, что слишком много факторов играют роль.

При исследовании эффекта Мпембы важно учитывать способ хранения воды, наличие примесей, положение термометра при замере.
Что произойдет, если провести максимально контролируемый эксперимент?
В 2016 году специалисты по динамике жидкостей инженер Генри Барридж, профессор Имперского колледжа Лондона, и математик Пол Линден из Кембриджского университета провели максимально контролируемое исследование эффекта Мпембы.
Они не нашли никаких свидетельств его существования, но не это главное. Самое существенное их открытие заключалось в том, что если буквально на сантиметр сместить положение термометра в емкости, не меняя никаких других условий, то небольшой эффект Мпембы появляется. Последующая проверка предыдущих исследований показала, что и там наблюдаемый эффект был в пределах погрешности.

Ученые продолжают экспериментировать?
Да, исследования продолжаются. Ученые ищут и изучают эффект Мпембы в различных веществах и условиях.
Подведем итог. Чисто физически у воды нет эффекта Мпембы, но в реальной жизни из-за твердых и газообразных примесей, материала, из которого сделаны емкости, особенностей морозильной камеры и многих других факторов горячая вода действительно может замерзать быстрее холодной.
Может быть интересно:
Стань частью сообщества Homo Science!
Зарегистрируйся чтобы получить 350 приветственных
баллов и открыть полный доступ к курсам,
тренажерам и конкурсам.
Почему вода замерзает? Описание, фото и видео

Силы и частицы
Вода – это вещество, которое может наблюдаться в трех агрегатных состояниях. Она может замерзать и быть твердым льдом, она бывает в жидкой форме, и также она присутствует в виде пара – не только в бане, но и в небе, в виде облаков. Однако в рамках данной статьи остановимся на первом ее состоянии, твердом.
Вода замерзает, образуя кристаллики твердого льда. Лед может формировать многокилометровые поверхности, покрывая реки, озера и другие водоемы. При этом он оказывается легче жидкой воды и всегда находится сверху. Замерзает вода из-за понижения температур.
Температуры и агрегатное состояние веществ
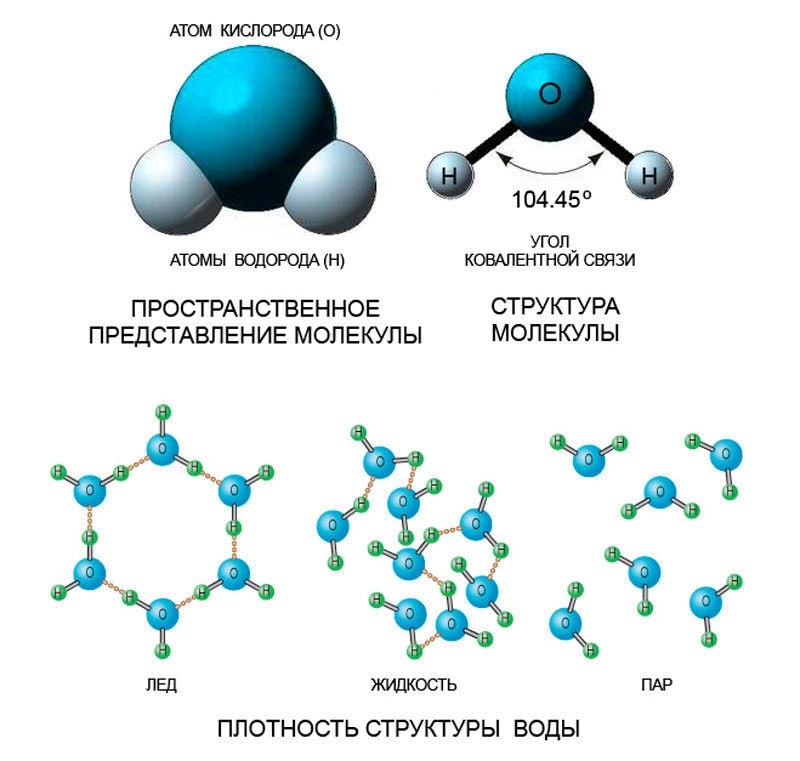
Молекула воды в различных агрегатных состояниях
Чем выше температуры, тем дальше отстоят между собой молекулы любых веществ. Их отдаление друг от друга приводит к размягчению вещества, которое сначала становится жидким, а потом и вовсе газообразным. Этот процесс можно рассмотреть на примере железа, которое плавится в тигле и обретает жидкую форму. При сильном повышении температур оно может стать и газообразным, то есть, испариться, но для этого температура должна быть по-настоящему высокой.
Вода же при обычной комнатной температуре является жидкостью. При повышении температур она станет паром, а при понижении – льдом. Ведь понижение температуры имеет обратное влияние на молекулы – они сближаются. А при их сближении вещество становится тверже, плотнее. Такого же эффекта можно добиться при механическом прессовании любого вещества- оно станет тверже, опять же из-за сближения молекул.
Что происходит при понижении температур?
Когда на воду оказывается влияние пониженных температур, молекулы сближаются, образуя шестигранные формы. Разумеется, это снежинки, которые являются кристаллами воды. Остывание воды и ее кристаллизация – это фактически синонимы, описывающие один и тот же процесс. Вода начинает кристаллизоваться при температуре в 0 градусов – именно этот момент и взят за нулевую отметку по шкале Цельсия. Если рассматривать американскую шкалу Фаренгейта, то здесь застывание воды будет происходить при 32 градусах.
Но для создания кристаллов воды нужна основа, какие-либо примеси или взвеси, благодаря которым стартует этот процесс. И если вода абсолютно чистая, здесь наблюдается несколько другое явление – порой она застывает только при -40 градусах, а при нуле и других не слишком низких отметках остается жидкой. Однако не замерзает она только в спокойном состоянии. Если ее взболтать при минусовых отметках, она немедленно превратится в лед.
С водой связано множество парадоксов. И кроме уже описанного выше нюанса, необходимо отметить, что лед занимает больше объема, чем жидкая вода, то есть, при замерзании это вещество расширяется, в то время как другие наоборот занимают меньше объема при низких температурах. Именно с расширением воды при формировании льда и связано лопание бочек, труб и других объектов, оставленных на зиму заполненными водой.
На момент замерзания молекулы немного отдаляются друг от друга, что и дает такой эффект. И именно этот фактор, наряду с вмерзшими пузыриками воздуха, делает лед плавучим. Если бы он тонул или формировался со дна, ни одно живое существо в водоемах не смогло бы перезимовать. Но формируясь именно на поверхности, и оставаясь там, лед наоборот сохраняет тепло воды и выполняет защитную функцию в зимнее время, давая животным, растениям и рыбам возможность перезимовать и выжить.
Если Вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
При какой температуре замерзает вода?
Температура замерзания воды зависит от давления. В так называемой тройной точке, когда в равновесии находятся все три фазы — лед, вода и водяной пар — температура равна плюс одна сотая градуса Цельсия, давление 611 Па. При атмосферном давлении 101325 Па (760 мм рт.ст.) температура замерзания воды равна 0,00 градуса Цельсия. При повышении давления температура замерзания воды может существенно снизиться. Например, под коньком конькобежца лед плавится даже в сильный мороз, что и позволяет коньку скользить по поверхности льда. Из северного цикла рассказов и повестей Джека Лондона мы знаем, что тяжело груженые нарты, если они долго стоят на месте, примерзают полозьями к дороге. Механизм этого явления такой — снег под полозьями плавится, нарты погружаются в снег, вытесняя наверх воду, вытесненная вода замерзает.
Концентрированные растворы любых веществ воде замерзают также при довольно низкой температуре (минус 20 — 30 градусов Цельсия и ниже), но это отдельный разговор. Вопрос был о воде, а не о водных растворах. Незначительные концентрации солей, как в питьевой воде, мало сказываются на температуре замерзания — понижают её на доли градуса. Морская вода замерзнет при минус 1 — 2 градуса.